![]()


Ill. Niklas Elmehed. © Nobel Media.
获奖原因
动物需要氧气才能将食物转化成有用的能量,自从现代生物学出现以来,人们就知道了维持生命需要氧气; 但是,细胞如何适应氧气供应变化的分子机制还不清楚。威廉·凯林、彼得·拉特克里夫爵士和格雷格·塞门扎发现了“细胞如何感知和适应不断变化的氧气供应”,并确认了“能够调节基因活性以适应不同氧气水平的分子机制”。今年的三名获奖科学家开创性的研究成果“揭示了生命中一个最基本的适应性过程的机制”,为我们理解氧气水平如何影响细胞新陈代谢和生理功能奠定了基础。他们的发现也为有望对抗贫血、癌症和许多其他疾病的新策略铺平了道路。
氧气:动物生命所必需

© The Nobel Committee for Physiology or Medicine. Ill. Mattias Karlén
氧是动物生命所必需的:在氧化反应中,氧化反应推动食物中的营养物质转化为能量。1931年诺贝尔生理学或医学奖的获得者奥托·沃伯格(Otto Warburg)发现有关细胞呼吸酶的基础。
生物为确保组织和细胞能够获得充足的氧气供应。生物在进化过程中逐渐演化出了一种机制:两侧颈部大血管附近的颈动脉体中含有一些特殊细胞,能够感知血液中的氧气水平。1938年诺贝尔生理学奖或医学奖得主科奈尔·海门斯发现了颈动脉体感知到的血氧水平如何与大脑直接交流、进而控制呼吸速率。
除了颈动脉体快速适应低氧水平(缺氧)外,还有其他基本的生理适应。缺氧的一个关键生理反应是促红细胞生成素(EPO)水平的升高,促红细胞生成素会增加红细胞的生成。激素控制红细胞的重要性在20世纪初就已为人所知,但该过程究竟如何受氧气水平所控制却一直未解。
缺氧诱导因子“HIF”的发现
Gregg L. Semenza研究了EPO基因,以及不同的氧气水平对该基因的调节过程。通过基因修饰的小鼠,发现位于EPO基因旁的特定DNA片段介导了对缺氧的反应。Peter J. Ratcliffe也研究了EPO基因的氧气依赖调节。两个研究小组都发现,几乎所有组织中都存在氧感应机制,而不仅仅是在通常产生EPO的肾脏细胞中。研究发现,该机制在许多细胞类型中广泛存在、且均能发挥作用。Gregg L. Semenza希望找出介导这种反应的细胞成分。在人工培养的肝细胞中,发现了一种调节这些依赖氧反应的转录因子,它以一种依赖氧的方式与DNA片段结合。他将该复合体称作“缺氧诱导因子”(HIF)。1995年,Semenza表明HIF转录因子是由两个部分组成的:HIF-1α和ARNT。氧气感知和适应机制
当动物细胞周围的氧气水平发生变化时,它们的基因表达就会发生根本的变化。这些基因表达的改变改变了细胞的新陈代谢、组织的重新建模,甚至改变了机体的反应,如心率和换气次数的增加。
一些研究表明,HIF-1α通常会迅速降解,但缺氧会对其起到保护作用。当氧气含量很高时,细胞中HIF-1α含量很低。当氧含量低时,HIF-1α的含量增加,使其可以结合基因位点,从而调节促红细胞生成素(EPO)基因以及其他基因与HIF结合DNA片段。
在Semenza和Ratcliffe探索EPO基因调控的同时,癌症研究员William Kaelin,Jr.正在研究一种遗传综合征,即von Hippel-Lindau病(VHL病)。这种遗传疾病会导致遗传性VHL突变的家庭罹患某些癌症的风险急剧增加。Kaelin表明,VHL基因编码一种可预防癌症发作的蛋白质,缺乏功能性VHL基因的癌细胞会异常高水平表达低氧调节基因。但是当VHL基因重新引入癌细胞后,恢复了正常水平。这是一个重要的线索,表明VHL以某种方式参与了对缺氧反应的控制。Ratcliffe和他的研究小组做出了一个关键发现:证明VHL可以与HIF-1α物理相互作用,并且是正常氧水平下降解所必需的。
氧气感知和适应机制描述
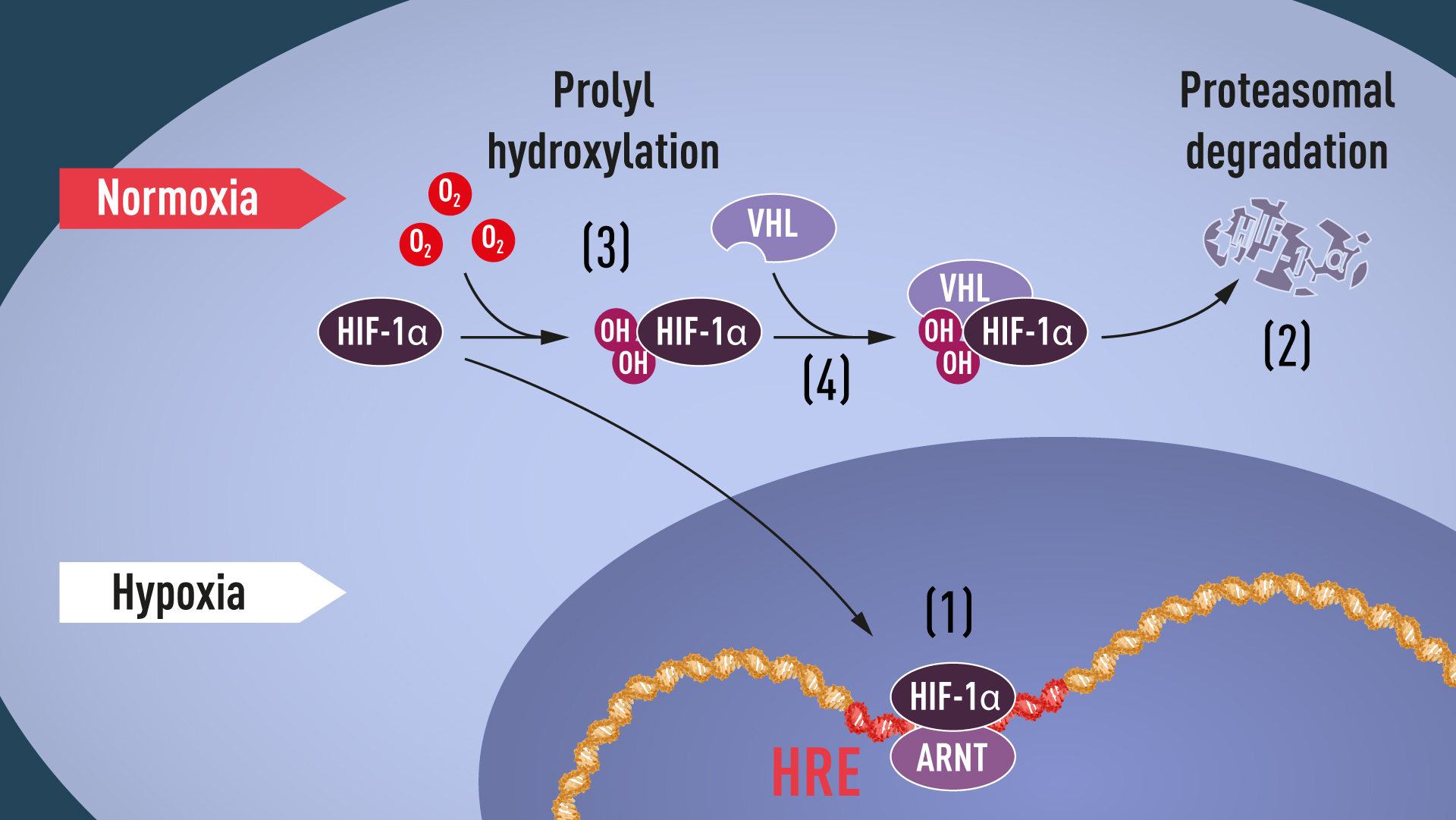
图片来源:https://www.nobelprize.org/prizes/medicine/2019/press-release/
在氧含量充足的情况下,蛋白酶体细胞器会降低HIF-1α的含量。HIF-α亚基在脯氨酸残基上被依赖于氧的脯氨酰-4-羟化酶 (PHD) 羟基化共价修饰(3)。脯氨酸羟化可让它结合VHL蛋白(4),在这种条件下,泛素(ubiquitin)被添加到HIF-1α蛋白质中,这是一种可靶向 HIF-α进行蛋白酶体降解的E3泛素-连接酶,将蛋白酶体降解(2)。在缺氧的情况下,FIH 活性受底物限制,导致 HIF-α 快速聚集、核转位以及与HIF-1β发生二聚化(1)。在HIF-1结合靶基因启动子内的 DNA 共有序列(定义为缺氧应答元件 [HRE])时,会发生反式激活。HIF-1会促进参与细胞自主和非自主适应缺氧的数百种基因的表达。HIF-1会对癌细胞和基质细胞产生多效性作用。例如,依赖于HIF-α的VEGF-A和PDGF-B 表达会促进周皮细胞、内皮细胞和血管平滑肌细胞的增殖和迁移,从而诱导血管生成。在癌症相关的成纤维细胞(CAF) 中,HIF-α介导细胞外基质 (ECM) 重构和代谢重新编程,从而支持细胞存活。通过这三位获奖者的共同工作,证明了基因表达对氧变化的反应与动物细胞内的氧水平直接相关,允许通过HIF转录因子的作用使细胞对氧化反应迅速应答。
Bioss 氧气感知和适应研究相关靶标产品
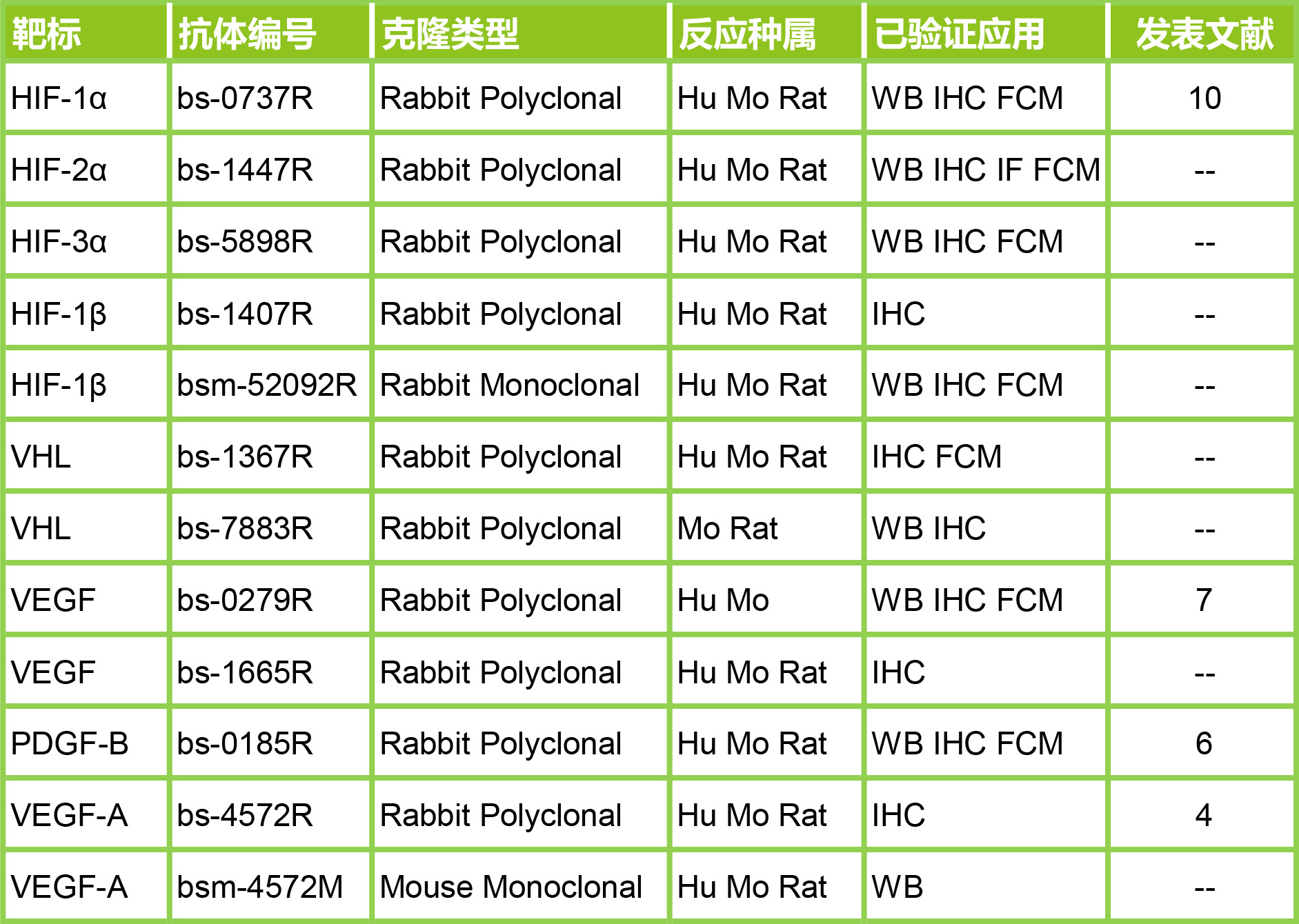
产品展示:
HIF-2α (bs-1447R)
Mouse Brain
HIF-1β (bs-1407R)
Mouse Uterus
VHL (bs-1367R)
Human kidney
VEGF (bs-0279R)
Mouse Heart Hela cells
VEGF-A (bs-4572R)
Rat Brain
参考文献
1.Mircea, I., Kondo, K., Yang, H., Kim, W., Valiando, J., Ohh, M., Salic, A., Asara, J.M., Lane, W.S. & Kaelin Jr., W.G. (2001) HIFa targeted for VHL-mediated destruction by proline hydroxylation: Implications for O2 sensing. Science, 292, 464-468
2.Jaakkola, P., Mole, D.R., Tian, Y.-M., Wilson, M.I., Gielbert, J., Gaskell, S.J., von Kriegsheim, A., Heberstreit, H.F., Mukherji, M., Schofield, C.J., Maxwell, P.H., Pugh, C.W. & Ratcliffe, P.J. (2001). Targeting of HIF-α to the von Hippel-Lindau ubiquitylation complex by O2-regulated prolyl hydroxylation. Science, 292, 468-472